医疗器械软件描述文档及体系文件模板word版doc 可编辑版|百度网盘下载
编者评论:医疗器械管理的基本文件
医院或专门组织医疗器械的朋友必备的模板文件。 医疗器械软件描述文档和系统文件模板word版是最新的完整版,支持编辑,可以直接编辑然后打印超级方便实用。
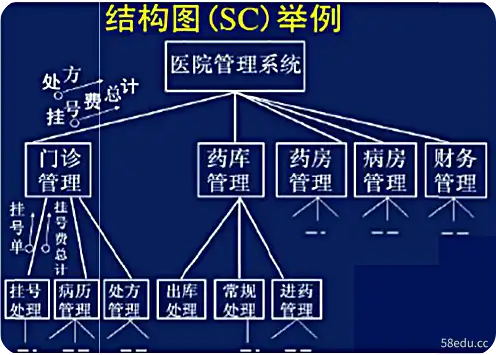
内容预览
1.1、产品标识
软件名称:
软件模型:
软件版本号:
软件制造商:
软件生产地址:
1.2、安全等级
软件的安全级别为 A/B/C。原因如下:
a) 软件的预期用途是
b) 软件的功能包括:
c) 如果软件出现故障,可能会导致以下后果(一一描述软件的每一个功能故障,如果硬件降低了软件故障时的故障后果或危害发生的概率,可以进行解释,并相应降低安全级别):
1)
2)
3)
医疗器械软件描述文档及系统图片预览





开箱即用的软件录制说明
根据国家食品药品监督管理总局2015年8月5日发布的《国家食品药品监督管理总局关于印发医疗器械软件注册技术审评指导原则(2015年第50号)的通知》第三类包括软件 对于医疗器械产品,无论软件开发方式是自行开发、部分使用现成软件还是全部现成软件,首次注册时均应提交软件说明文件.软件描述文档的详细程度、术语和要求根据安全级别和开发方式而有所不同。
对于自主开发的医疗器械软件,软件描述文档包括基本信息、实现过程和核心算法(详见附件)。
部分使用现成的软件
对于现成的方法,三个现成的软件要求不同:
成品软件:如果成品软件已在中国上市,则制造商应提供外包合同或声明副本、软件说明文件(不适用于条款和理由)、注册证书副本;
旧版软件:厂商应提供旧版软件证明文件(如YY/T 0664或IEC 62304实施前的注册证或上市批准复印件)、软件说明文件(不适用条款说明原因)、上市后临床评价数据;
外包软件:制造商应提供外包合同或声明、软件说明文件的副本(不适用条款说明原因)。
阅读剩余
版权声明:
作者:伍小杰
链接:https://www.58edu.cc/article/1523036662844620802.html
文章版权归作者所有,58edu信息发布平台,仅提供信息存储空间服务,接受投稿是出于传递更多信息、供广大网友交流学习之目的。如有侵权。联系站长删除。
作者:伍小杰
链接:https://www.58edu.cc/article/1523036662844620802.html
文章版权归作者所有,58edu信息发布平台,仅提供信息存储空间服务,接受投稿是出于传递更多信息、供广大网友交流学习之目的。如有侵权。联系站长删除。
THE END